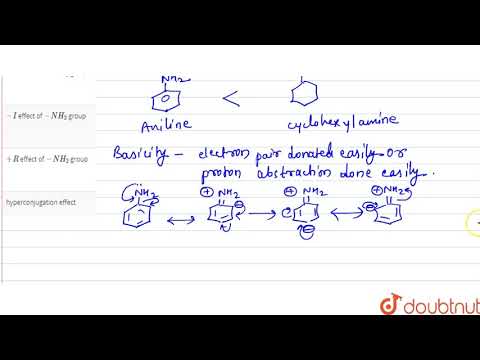
چرا آنیلین باز ضعیف تر از سیکلوهگزیلامین است؟ در آنیلین (C6H5NH2)، گروه فنیل (C 6H5) یک گروه الکترون خارج کننده است و بنابراین دسترسی الکترون در نیتروژن را کاهش می دهد - NH2 گروه و در نتیجه آن را به پایه ضعیف تری تبدیل می کند.
چرا آنیلین یک پایه ضعیف است؟
آنیلین فقط با اکراه پروتون را می پذیرد تا یون آنیلینیوم را تشکیل دهد و از این رو یک باز ضعیف است. هنگامی که یک گروه -NH به یک رادیکال آلیفاتیک متصل می شود، هیچ تثبیت محلی سازی قابل مقایسه ای دریافت نمی کند. تمایل کمتری به پذیرش پروتون روی جفت نیتروژن خود ندارد و از این رو آمین های آلیفاتیک بازهای قوی تری هستند.
آیا آنیلین اسیدی تر از سیکلوهگزیلامین است؟
متن تصویر رونویسی شده: سیکلوهگزیلامین اساسیتر از آنیلین است زیرا: آنیلین میتواند هیدروژن کمتری اهدا کند. الکترونهای روی نیتروژن آنیلین تا حدودی در حلقه معطر جابجا میشوند.
آنیلین پایه قوی تر است یا سیکلوهگزیلامین؟
در سیکلوهگزیل آمین، گروه سیکلوهگزیل (غیر معطر) یک گروه آزاد کننده الکترون است و بنابراین چگالی الکترون را در نیتروژن افزایش می دهد - NH2 گروهو آن را به یک پایه قوی تر از آنیلین تبدیل می کند (اثر القایی).
چرا آنیلین باز ضعیف تر از آمونیاک است؟
اساساً آنیلین به عنوان ساده ترین آمین معطر در نظر گرفته می شود. در حال حاضر، آنیلین به عنوان یک باز ضعیف تر از آمونیاک در نظر گرفته می شود. این به دلیل این واقعیت است که جفت تنها در آنیلین در رزونانس با حلقه بنزن درگیر است و بنابراین به اندازه در NH3 برای اهدا در دسترس نیست.