از آنجایی که سلولهای گالوانیکی خودبهخود هستند، برای تبدیل شدن به سلول الکترولیتی نیاز به کسب انرژی دارند. علاوه بر این آند و کاتد سلول گالوانیکیسوئیچ می شوند و واکنش به صورت معکوس انجام می شود به طوری که سلول گالوانیکی به سلول الکترولیتی تبدیل می شود.
وقتی یک سلول گالوانیکی به یک سلول الکترولیتی تبدیل می شود چه اتفاقی می افتد؟
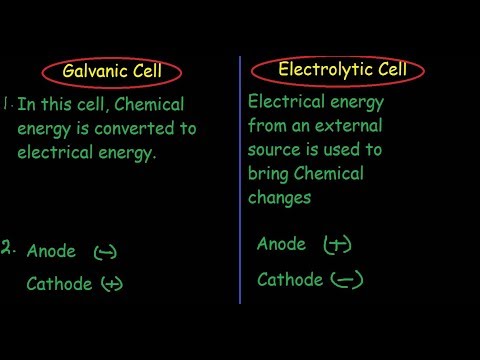
یک سلول گالوانیکی انرژی شیمیایی را به انرژی الکتریکی تبدیل می کند یک سلول الکترولیتی انرژی الکتریکی را به انرژی شیمیایی تبدیل می کند. در اینجا، واکنش ردوکس خود به خود است و مسئول تولید انرژی الکتریکی است. … واکنش در آند اکسیداسیون و در کاتد کاهش است.
آیا سلول های گالوانیکی سلول الکترولیتی هستند؟
دو نوع سلول الکتروشیمیایی وجود دارد: سلول های گالوانیکی که ولتاییک نیز نامیده می شود، و الکترولیتی سلول های گالوانیکی انرژی خود را از واکنش های ردوکس خود به خود به دست می آورند، در حالی که سلول های الکترولیتی شامل واکنش های غیر خود به خودی و بنابراین به یک منبع الکترونی خارجی مانند باتری DC یا منبع برق AC نیاز دارید.
چه چیزی یک سلول را الکترولیتی می کند؟
یک سلول الکترولیتی یک سلول الکتروشیمیایی است که از انرژی الکتریکی برای هدایت یک واکنش ردوکس غیر خود به خودی استفاده می کند… یک سلول الکترولیتی دارای سه بخش است: یک الکترولیت و دو الکترود (یک کاتد و آند). الکترولیت معمولاً محلولی از آب یا سایر حلالها است که یونها در آن حل میشوند.
چگونه آند و کاتد را در یک سلول الکترولیتی شناسایی می کنید؟
اگر می بینید که کاهش سلول گالوانیکی در الکترود سمت چپ اتفاق می افتد، بنابراین سمت چپ کاتد استاکسیداسیون در الکترود سمت راست انجام می شود، بنابراین الکترود مناسب آند است. در حالی که در سلول الکترولیتی کاهش در الکترود سمت راست صورت می گیرد، بنابراین الکترود سمت راست کاتد است.