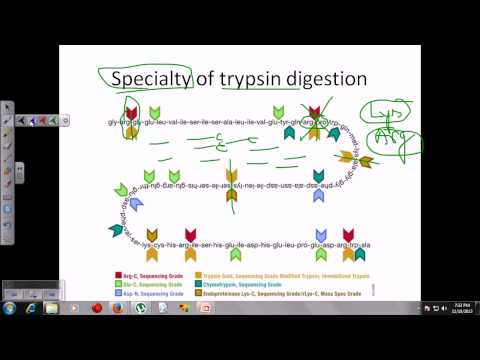
تریپسین پیوند پپتیدی بین گروه کربوکسیل آرژنین یا گروه کربوکسیل لیزین و گروه آمینه اسید آمینه مجاور را قطع می کند. هنگامی که بقایای لیزین و آرژنین در مجاورت اسیدهای آمینه اسیدی در توالی یا سیستین قرار دارند، سرعت برش کندتر اتفاق میافتد.
تریپسین در کجا اسیدهای آمینه را می شکافد؟
تریپسین پپتیدها را در سمت C ترمینال باقی مانده های اسید آمینه لیزین و آرژنینمی شکافد. اگر باقیمانده پرولین در سمت کربوکسیل محل برش باشد، برش رخ نخواهد داد.
تریپسین چه دنباله ای را قطع می کند؟
Trypsin منحصراً C ترمینال را به باقی مانده های آرژنین و لیزین می شکافد. جمعیت ها.
تریپسین و کیموتریپسین با چه آمینواسیدهایی قطع می کنند؟
تریپسین لیزین و آرژنین را کاهش می دهد در حالی که کیموتریپسین. تیروزین، فنیل آلانین و تریپتوفان را کاهش می دهد. چگونه آنزیم می داند که در آنجا برش دهد؟ یک جایگزین برای آسپارتات و هیستیدین در سه گانه کاتالیزوری پیشنهاد کنید.
پپسین چه اسیدهای آمینه ای را می شکافد؟
پپسین پیوندهای پپتیدی را در سمت آمینه پایانی باقیمانده های اسید آمینه حلقوی ( تیروزین، فنیل آلانین و تریپتوفان می شکند)، زنجیره های پلی پپتیدی را به پپتیدهای کوچکتر می شکند (Fange و گروو، 1979).